Afatinib được FDA phê duyệt điều trị ung thư phổi tế bào vảy dựa trên nghiên cứu LUX-Lung 8
04/07/2025 10:41:23
1. Mở đầu – Bước ngoặt trong điều trị ung thư phổi tế bào vảy
Ung thư phổi tế bào vảy (Squamous Cell Carcinoma – SCC) là một dạng ung thư phổi không tế bào nhỏ (NSCLC) phổ biến ở nam giới lớn tuổi, thường liên quan đến hút thuốc lá kéo dài. Trong nhiều năm, điều trị SCC chủ yếu dựa vào hóa trị hoặc miễn dịch, với hiệu quả còn hạn chế.
Sự xuất hiện của Afatinib (Giotrif, Afanat) – một thuốc TKI thế hệ thứ 2 – mang lại một lựa chọn mới. Đặc biệt, sau kết quả tích cực từ nghiên cứu LUX-Lung 8, FDA đã phê duyệt Afatinib (năm 2018) để điều trị SCC giai đoạn tiến triển.

2. Afatinib – từ điều trị EGFR đến mở rộng sang SCC
Ban đầu, Afatinib được sử dụng trong điều trị NSCLC có đột biến EGFR. Tuy nhiên, Afatinib có cơ chế ức chế không hồi phục trên toàn bộ họ ErbB (EGFR/HER1, HER2, HER4) – điều mà các TKI thế hệ 1 như Erlotinib không làm được.
Chính đặc tính này giúp Afatinib hiệu quả ở cả ung thư phổi tế bào vảy, dù nhóm này hiếm khi mang đột biến EGFR truyền thống.
3. Nghiên cứu LUX-Lung 8 – Bằng chứng khoa học thuyết phục
LUX-Lung 8 (NCT01523587) là một thử nghiệm lâm sàng pha III so sánh trực tiếp giữa Afatinib và Erlotinib trên 795 bệnh nhân SCC giai đoạn tiến triển, đã thất bại với hóa trị bạch kim trước đó.
Số người tham gia:
398 dùng Afatinib
397 dùng Erlotinib
Kết quả chính:
Thời gian sống không bệnh tiến triển (PFS):
Afatinib: 2,4 tháng
Erlotinib: 1,9 tháng
→ Afatinib vượt trội (HR 0.82, p = 0.0427)
Thời gian sống toàn bộ (OS):
Afatinib: 7,9 tháng
Erlotinib: 6,8 tháng
→ Tăng sống thêm trung bình 1,1 tháng (HR 0.81, p = 0.0077)
Chất lượng sống:
Bệnh nhân dùng Afatinib báo cáo cải thiện đáng kể triệu chứng ho, đau, khó thở và thể trạng chung so với Erlotinib
Ý nghĩa: Đây là lần đầu tiên một TKI cho thấy hiệu quả vượt trội trên SCC không phụ thuộc đột biến EGFR.
4. FDA phê duyệt mở rộng chỉ định
Dựa vào kết quả nghiên cứu trên, FDA chính thức phê duyệt Afatinib vào năm 2018 cho chỉ định:
Điều trị bệnh nhân ung thư phổi tế bào vảy (SCC) giai đoạn tiến triển, sau khi thất bại với hóa trị.
Điều này giúp mở rộng lựa chọn điều trị bước 2 cho nhóm bệnh nhân SCC vốn có rất ít liệu pháp nhắm đích hiệu quả.
5. Cách sử dụng Afatinib ở bệnh nhân SCC
Liều khuyến cáo: 40mg/lần/ngày, uống trước ăn ít nhất 1 giờ hoặc sau ăn 2 giờ
Có thể giảm liều xuống 30mg hoặc 20mg tùy mức dung nạp
Không yêu cầu xét nghiệm đột biến EGFR để dùng trong SCC
6. Tác dụng phụ – điểm cần lưu ý
So với Erlotinib, Afatinib có tỷ lệ tác dụng phụ cao hơn, tuy nhiên phần lớn có thể kiểm soát được:
Tiêu chảy (phổ biến nhất): dùng Loperamide sớm để ngăn biến chứng
Phát ban, ngứa, khô da
Loét miệng
Mệt mỏi, chán ăn
Bệnh nhân cần được theo dõi sát và điều chỉnh liều khi cần thiết.
7. Afatinib – lựa chọn hữu ích trong điều trị bước 2 SCC
Afatinib mang lại nhiều lợi ích:
✅ Hiệu quả điều trị vượt trội hơn Erlotinib
✅ Không yêu cầu đột biến gen – mở rộng cơ hội cho nhiều bệnh nhân hơn
✅ Giúp kéo dài sống thêm, cải thiện triệu chứng và chất lượng sống
✅ Phù hợp với bệnh nhân sau khi thất bại hóa trị hoặc miễn dịch
Kết luận
Afatinib không chỉ là thuốc điều trị nhắm đích trong NSCLC có đột biến EGFR, mà còn là giải pháp hiệu quả bước 2 cho bệnh nhân ung thư phổi tế bào vảy. Nhờ kết quả tích cực từ nghiên cứu LUX-Lung 8, thuốc đã được FDA phê duyệt mở rộng chỉ định, mở ra hy vọng mới cho nhóm bệnh nhân vốn ít lựa chọn điều trị.
Trong bối cảnh tỷ lệ SCC vẫn còn cao tại Việt Nam, việc cập nhật thông tin và ứng dụng Afatinib đúng cách là một bước đi quan trọng trong cá nhân hóa điều trị ung thư phổi.
-
Bác sĩ Hỗ Trợ Mùa Dịch
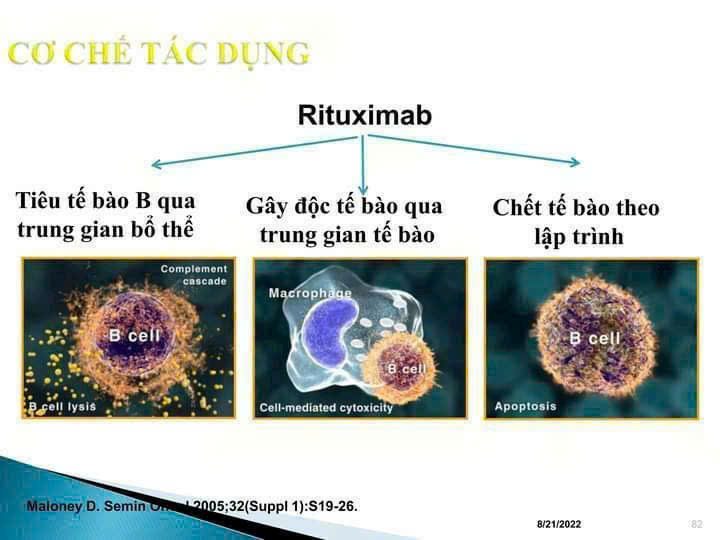
Giải pháp điều trị hiệu quả cho các bệnh ung thư và rối loạn miễn dịch
 20/06/2025
20/06/2025
-
Bác sĩ Hỗ Trợ Mùa Dịch
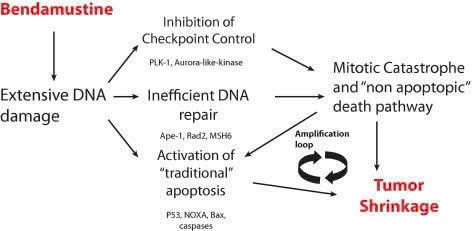
Thuốc hóa trị nhóm alkyl hóa hiệu quả trong điều trị ung thư huyết học
 20/06/2025
20/06/2025
-
Bác sĩ Hỗ Trợ Mùa Dịch
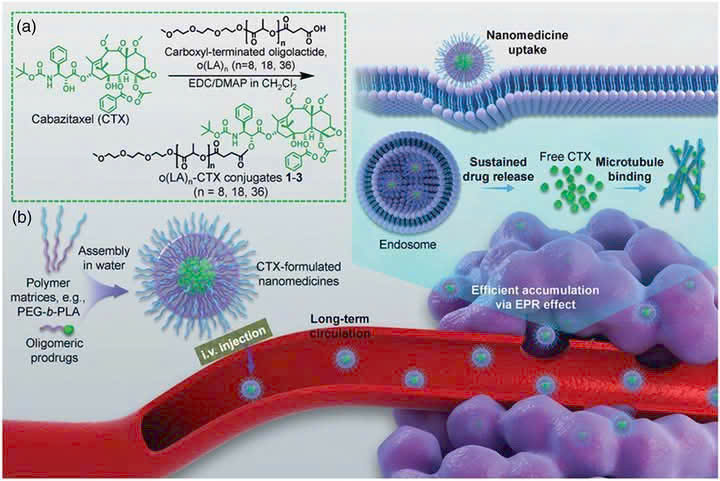
Lựa chọn điều trị ung thư tuyến tiền liệt di căn kháng thiến sau Docetaxel
 20/06/2025
20/06/2025

Xem danh sách nhà thuốc trên toàn quốc

-

Duy Nguyễn Nhất





Rất tuyệt vời, đặc biệt trong mùa dịch đi lại khó khăn. Chúc tdoctor ngày càng phát triển và mở rộng phạm vi ra nhiều tỉnh hơn, nhất là vùng Đồng bằng sông Cửu Long.
-

Quốc Bình Vũ





Ứng dụng rất hay. Giúp mọi người hạn chế bệnh gì cũng phải đến bệnh viện khám. Đỡ mất thời gian, công sức và tiền bạc vì nhiều khi vô gặp bs cũng chỉ cần hỏi vài câu và cho SP.
-

Nguyễn Ngọc Minh





Em bị ung thư thấy bác sĩ tuyến trung ương trong hệ thống tdoctor, bác sĩ bên tdoctor rất nhiệt tình, rất tiện cho trường hợp mua sản phẩm dược và thực phẩm chức uy tín online.